Le titre même de sa présentation et le grand nombre de participation ne laissait aucun doute sur sa pertinence : "quels médicaments lors d'une grossesse ?" La question est à double tranchant à savoir de déterminer les risques pour la mère de ne pas la traiter et ceux pour l'enfant en cas de traitement.

Pour Monika Østensen, il existe plusieurs moments qui doivent être considérés. "La prise en charge d'une patiente souffrant d'une maladie rhumatismale débute déjà bien avant la grossesse où il faudra stopper toutes les molécules que l'on sait tératogène et poursuivre celles qui permettent de maintenir une rémission. Il faudra aussi expliquer à la patiente pourquoi. Ainsi, le mycophénolate et le méthotrexate (MTX) sont connus pour augmenter le risque de malformations de 3 à 5%, par exemple", insiste la Norvégienne.
Risque accru
L'étude de Weber-Schoendorfer et de ses collègues (1) a montré que l'exposition au MTX 0 à 10 semaines avant la conception engendrait un taux de fausses couches de 14,4% et de malformations dans 3,5%. Si le traitement a lieu au cours du premier trimestre, le taux de fausses couches est de 42,5% et de malformations de 6,6% versus 2,9% dans la population générale et 3,5% dans une population de femmes présentant une maladie rhumatismale non traitées par MTX. "Il faut donc arrêter la prise de MTX 1 à 3 mois avant la conception, 3 mois avant pour le cyclophosphamide et 6 semaines avant pour le mycophénolate", précise-t-elle. La règle est de ne pas entamer ce type de traitement sans s'assurer qu'une contraception efficace est mise en oeuvre. Par ailleurs, il existe des alternatives puisque les antimalariques, la sulfasalazine, l'azathioprine, la ciclosporine, de faibles doses de prednisone, les inhibiteurs TNF et le tacrolimus n'augmentent pas le risque tératogène, ni les AINS aux premier et deuxième trimestres.
Ces derniers peuvent néanmoins engendrer le développement d'une hypertension artérielle pulmonaire chez le foetus s'ils sont administrés en trop grandes quantités ; ils peuvent aussi provoquer une déficience rénale foetale avec la formation d'un oligohydroamnios. Ces effets sont dose-dépendants, mais sont heureusement réversibles à l'arrêt du traitement. Concernant les corticostéroïdes, la spécialiste scandinave conseille de maintenir une dose inférieure à 10 mg/j et de traiter les accès par de hautes doses à court terme. "Ces médicaments peuvent engendrer des effets chez la mère, notamment une augmentation du risque infectieux et chez l'enfant avec un retard de croissance et une augmentation du risque de prématurité."
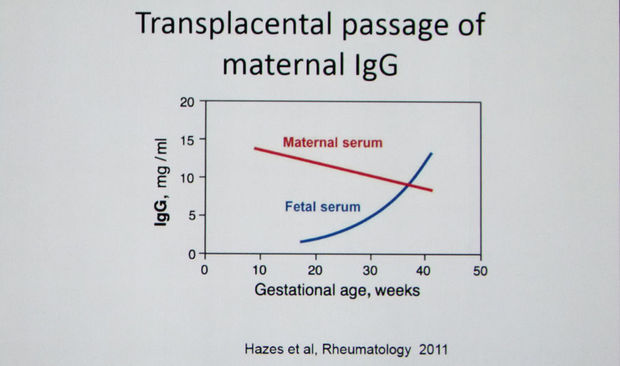
Biologiques : moins de danger ?
Les traitements biologiques mériteraient un article à eux seuls. Leurs effets dépendent de leur structure, de leur demi-vie et de l'affinité pour le récepteur foetal Fc pour les immunoglobulines. La spécialiste a d'ailleurs publié un article à ce sujet cette année. (2) On y voit par exemple que l'infliximab a un ratio foeto-maternel de 2,2, c'est-à-dire que le foetus concentre la molécule alors que l'étanercept a un ratio de 0,5 et le certolizumab de 0. "Néanmoins, les méta-analyses publiées à ce sujet ne montrent pas de différences au moment de la naissance par rapport à la population générale. (3,4)" Cependant, si le traitement s'est poursuivi durant la fin du 3ème trimestre, les enfants ne devraient pas recevoir de vaccins vivants atténués durant les 6 premiers mois de vie. Néanmoins, des résultats préliminaires ne montrent pas d'augmentation du risque d'infection au cours de la première année.
Enfin, certains médicaments font partie de la zone grise, car les données scientifiques manquent encore à ce sujet. Le meilleur conseil est de les éviter durant la grossesse ou d'en réduire le dosage au minimum. Pour le leflunomide, un wash-out est conseillé même si une étude menée sur 45 patientes n'a pas montré d'augmentation de risque. Les autres médicaments entrant dans cette catégorie sont le rituximab, le belimumab, l'abatacept, le tocilizumab, l'anakinra et l'ustekinumab. D'autres sont tellement nouveaux qu'il est impossible à l'heure actuelle d'en dire quoi que ce soit comme le tofacitinib, le baricitinib, le secukinumab et le canakinumab. "Ils devraient être évités chez la patiente enceinte", avertit Ostensen. Qu'en est-il des papas alors ? Malgré la controverse, le MTX ne montre pas d'effets négatifs d'un traitement du père sur les malformations congénitales de l'enfant à naître.
L'essentiel pour la spécialiste est de pouvoir conseiller le mieux possible la famille en l'informant, mais aussi en collaborant avec tous les professionnels de la santé qui entourent la grossesse : gynécologues, obstétriciens, pédiatres, etc.
Østensen M. Which drugs in pregnant patients? EULAR 2017 Abstract#SP0112
Ref
- Weber-Schoendorfer et al. Pregnancy outcome after methotrexate treatment for rheumatic disease prior to or during early pregnancy: a prospective multicenter cohort study. Arthritis Rheumatol. 2014 May;66(5):1101-10.
- Østensen M. The use of biologics in pregnant patients with rheumatic disease. Expert Rev Clin Pharmacol. 2017 Jun;10(6):661-669.
- Skorpen CG et al. The EULAR points to consider for use of antirheumatic drugs before pregnancy, and during pregnancy and lactation l. Ann Rheum Dis 2016;0:1-16
- Y Komaki et al.Efficacy, Safety and Pharmacokinetics of Biosimilars of Anti-Tumor Necrosis Factor-α Agents in Rheumatic Diseases; A Systematic Review and Meta-Analysis J Autoimmun 2017 ; 79, 4-16.

